Agronomía Costarricense 49 (2025) 3584

Artículo científico
Biología del barrenador de raíces de piña Sufetula anania (Lepidoptera: Crambidae)
William Méndez-Leiva 1, Helga Blanco-Metzler2/*
*Autora para correspondencia. Correo electrónico: helga.blanco@ucr.ac.cr
1Agroindustrial Piñas del Bosque S.A.,
Departamento de Investigación y Desarrollo, San Carlos, Costa Rica. ![]() https://orcid.org/0009-0003-4087-5725
https://orcid.org/0009-0003-4087-5725
2Universidad de Costa Rica, Centro de
Investigación en Protección de Cultivos, San José, Costa Rica. ![]() https://orcid.org/0000-0001-9926-0424
https://orcid.org/0000-0001-9926-0424
DOI: https://doi.org/10.15517/dq584971
Recibido el 03 de febrero del 2025; Aceptado el 07 de julio del 2025
Introducción. La producción de piña fresca en Costa Rica es una actividad económica rentable que se realiza en la Región Huetar Norte. Recientemente, la planta ha sido afectada por una nueva plaga, Sufetula anania Solís y Hayden (Lepidoptera: Crambidae), la cual causa un daño irreversible a la planta, con capacidad de destruir el sistema radical. Objetivo. Determinar el ciclo de vida y aspectos biológicos del barrenador de las raíces Sufetula anania en el cultivo de piña en la Zona Norte de Costa Rica. Materiales y métodos. El estudio se realizó en el laboratorio del Departamento de Investigación y Desarrollo de la empresa Agroindustrial Piñas del Bosque S.A., San Carlos, Costa Rica. Se determinaron los principales aspectos biológicos: ciclo de vida, parámetros biométricos y se desarrolló una metodología de reproducción en el laboratorio. Resultados. S. anania tiene un ciclo de vida compuesto por 4 estados de desarrollo (huevo, larva, pupa y adulto) con una duración entre 29 y 70 días. La duración en días para cada estado fue: huevos (7,10 ± 0,02); larvas: L1 (3,10 ± 0,31), L2 (2,20 ± 0,48), L3 (2,77 ± 0,57), L4 (4,53 ± 1,72), L5 (11,30 ± 2,71), pupa (8,63 ± 1,3), hembra (7,29 ± 2,65) y macho (5,25 ± 4,27). Se describe la metodología de reproducción en laboratorio compuesta por secciones de tallos de semilla vegetativa de piña. Conclusión. S. anania puede completar entre 6 a 12 ciclos de vida al año dependiendo de las condiciones climáticas y disponibilidad de alimento. Durante la alimentación, las larvas generan túneles dentro de los tejidos vegetales que les sirven como sitios de refugio y protección.
Palabras clave: Sufetula anania; Crambidae; Ananas comosus; ciclo de vida.
Research Article
Abstract
Biology of the pineapple root borer Sufetula anania (Lepidoptera: Crambidae)
Introduction. Fresh pineapple production in Costa Rica is a profitable economic activity that is carried out in the Huetar Norte Region; it is recently affected by a new pest, Sufetula anania Solis and Hayden (Lepidoptera: Crambidae) which causes damage to the plant, with the capacity of destroying the root system. Objective. To determine the life cycle and ecology of the root borer S. anania in pineapple cultivation in the Northern Zone of Costa Rica. Materials and methods. The study was carried out in the laboratory of Research and Development, of Agroindustrial Piñas del Bosque Company, San Carlos, Costa Rica. Main biological aspects, life cycle and biometric parameters were determined and a breeding methodology was developed. Results. S. anania has a life cycle composed of 4 stages of development (egg, larva, pupa and adult) and is completed between 29 and 70 days; the duration in days of each life cycle stage was: eggs (7.10 ± 0.02), larvae: L1 (3.10 ± 0.31), L2 (2.20 ± 0.48), L3 (2.77 ± 0.57), L4 (4.53 ± 1.72), L5 (11.30 ± 2.71), pupae (8.63 ± 1.3), adults: female (7.29 ± 2.65) and male (5.25 ± 4.27). The laboratory breeding methodology was based on stem sections of vegetative pineapple suckers. Conclusion. S. anania can complete 6 to 12 life cycles per year depending on climatic conditions and food availability. During feeding, the larvae generate tunnels within the plant tissues that serve as places of refuge and protection.
Keywords: Sufetula anania; Crambidae; Ananas comosus; life cycle.
La producción de piña fresca en Costa Rica es una actividad productiva y de importancia socioeconómica. La piña fresca se ha consolidado como fruta de gran aceptación y sus exportaciones han mantenido un crecimiento sostenido hacia mercados altamente competitivos (Castro 2019). Actualmente, la Región Huetar Norte de Costa Rica representa el 53% de la producción nacional distribuida en 22 600 ha en donde se generan 28 000 empleos directos (CANAPEP 2024).
En el 2018, los productores de la Zona Norte de Costa Rica observaron un retraso en el crecimiento de algunas plantas de piña en la periferia de las plantaciones. Se detectó una larva diminuta que causaba un daño irreversible a la planta, con capacidad de destruir el sistema radical (SFE 2018). No se han publicado datos de las pérdidas asociadas con esta plaga. Sin embargo, los daños observados generan retrasos en el desarrollo vegetativo, entrada de agentes fitopatógenos que causan enfermedades y, finalmente, menor productividad y tonelaje. Cruz y Obando (2021) reportan que consumos acumulados de raíces por las larvas llegan a alcanzar hasta 440 mg día-1 larva-1. Bartholomew et al. (2003) señalaron que uno de los factores que afecta en mayor medida la uniformidad y el rendimiento del cultivo es el ataque de plagas de suelo durante los primeros tres meses de desarrollo de la plantación.
Solís et al. (2019) publicaron por primera vez la identificación de Sufetula anania Solís y Hayden (Lepidoptera: Crambidae) como plaga de las raíces de la planta de piña en Costa Rica. El género Sufetula Walker incluye 30 especies descritas que están distribuidas globalmente en bosques tropicales y subtropicales (Nuss et al. 2022). La especie más conocida como plaga de raíz en palma aceitera es Sufetula diminutalis (Walker) presente en La Florida, el Caribe, América Central, Colombia y Perú (Hayden 2013 y Genty y Mariau 1975). Otros dos reportes tratan únicamente sobre el control de Sufetula spp. en Indonesia (Bonneau et al. 2004, 2007).
Desde hace varias décadas, se ha consolidado la importancia de los estudios biológicos de los insectos (Nielsen 1998). Este conocimiento permite valorar el impacto de las plagas, así como descubrir y diseñar tácticas para su manejo (Hilje y Saunders 2008). Los estudios de carácter biológico deben basarse en el conocimiento de sus características como: ciclo de vida, reproducción, hábitos y preferencia alimentaria (Blanco-Metzler et al. 1993 y Vandermeer y Goldberg 2013).
A la fecha, hay escasas publicaciones sobre aspectos biológicos del S. anania; por ejemplo, la duración de los estados del ciclo de vida, comportamiento alimenticio, entre otros aspectos importantes. Asimismo, las metodologías para el proceso de cría y reproducción de S. anania son escasas, laboriosas y erráticas. Por lo tanto, en este estudio se determinaron los principales aspectos biológicos de S. anania: ciclo de vida, parámetros biométricos y se describe una metodología de crianza en laboratorio compuesta por secciones de tallos de semilla vegetativa de piña.
Materiales y métodos
Características de los sitios experimentales. El estudio de campo se desarrolló en la Compañía Agroindustrial Piñas del Bosque S.A., ubicada en San Carlos, Provincia de Alajuela, Costa Rica, (10 °23 ´368" N/ 84 °15 ´096" O), con una altura de 400 msnm. Según datos propios de la finca, el sitio presenta una precipitación anual promedio de 3000 mm, una temperatura promedio anual de 24 °C y una humedad relativa promedio de 85%. El estudio de laboratorio se realizó en el Laboratorio del Departamento de Investigaciones ubicado en la finca. La temperatura (grados Celsius) y humedad relativa (porcentaje) se registraron diariamente usando el medidor digital marca DeltaTrack modelo 13309.
Recolección de insectos en campo. Los adultos se recolectaron entre enero y agosto del año 2022. Se establecieron tres bloques de siembra para la recolección de los adultos. Cada sitio estuvo cercano a bosques secundarios o pastizales, donde se instalaron cinco parcelas que se mantuvieron libres de aplicaciones de insecticidas. El área de cada parcela fue de 168 m2 a 20 m entre sí; en su perímetro se colocó el atrayente P592-Lure (nombre químico: mezcla de aldehídos de 16 carbonos; fórmula molecular: C16H30O) de la compañía ChemTica Internacional S.A (Heredia, Costa Rica) diseñado para la atracción de S. anania.
Las capturas de los adultos de S. anania se realizaron durante la noche en los sitios descritos anteriormente. Se utilizaron telas blancas de tipo tergal y luces led blancas de alta intensidad (≥ 200 lúmenes). Los adultos vivos fueron recolectados dentro de botellas plásticas trasparentes de 1,5 L e, inmediatamente, se trasladaron al laboratorio para iniciar el proceso de reproducción y crianza.
Crianza de los individuos (huevos, larvas, pupas y adultos) con dieta natural en el laboratorio. La dieta natural para las larvas consistió en una porción interna del tallo de semilla vegetativa de la piña que se cambiaba cada cuatro días (Figura 1 A, B, y C). El tejido se lavó con agua potable y, posteriormente, se le realizó un tratamiento para evitar la contaminación. Se aplicó el fungicida fludioxonil al 23% por medio de una inmersión durante un minuto con una dosis de 2,6 mL L-1. La dieta natural con su tratamiento químico y los factores ambientales fueron elementos fundamentales para la metodología de crianza bajo condiciones de laboratorio. Durante el periodo del estudio, se registró un promedio de temperatura de 25,1 °C y una humedad relativa promedio de 83%; mientras que el fotoperiodo utilizado siguió las mismas condiciones ambientales de la Zona Norte de Costa Rica: aproximadamente 12 h luminosidad: 12 h oscuridad.
Huevos. Los adultos machos y hembras provenientes del campo se depositaron dentro de cámaras para la oviposición. Las cámaras consistieron en cajas plásticas transparentes de 30 cm de longitud, 15 cm de ancho y 7 cm de altura (Figura 1 D). Las cajas son fabricadas por la empresa Kendy (Concepción, Chile) bajo la codificación: plástico de tipo alimenticio N °5 (polipropileno). En el interior de las cámaras, también se colocaron porciones de hojas de plantas de piña y dieta natural con el propósito de fomentar la oviposición, así como un algodón con miel de abeja al 10% para la alimentación de los adultos. La recolección de los huevos se realizó a los cuatro días después del ingreso de los adultos a la cámara. A partir de este momento, se separaron los huevos en diferentes grupos según los objetivos del estudio.
Los huevos se colocaron dentro de envases plásticos redondos de 237 mL (Figura 1 E). Los envases plásticos eran de tipo alimenticio N °5 (polipropileno) y se taparon para evitar la depredación. Se colocó un trozo de papel filtro húmedo en el interior de los envases para evitar la desecación de los huevos, el cual se reemplazó cada dos días. Para facilitar el conteo de los huevos, se dibujó una cuadrícula en el papel filtro (Figura 1 F) y se trasladaron individualmente a la dieta (Figura 1 G). Los huevos se revisaron diariamente y se registró la duración (días) para la eclosión (huevo a larva del primer estadío), así como el porcentaje de huevos eclosionados. Se determinó la media (días), la desviación estándar (días), el ámbito (días) y el coeficiente de variación en un grupo de 30 huevos.
Además, se utilizó un segundo grupo de huevos, a los cuales se les midió el ancho y el largo. Se manejó como un grupo aparte con el objetivo de evitar que la luz del estereoscopio afectara la eclosión. Se determinó la media (mm), la desviación estándar (mm), el ámbito (mm) y coeficiente de variación en ese segundo grupo de 30 huevos.
Larvas. Se realizaron diferentes procesos de crianza con el propósito de alcanzar la totalidad de datos requeridos durante la etapa larval. Cada una de las larvas L1 recién emergidas se colocaron con un pincel fino dentro de envases plásticos redondos con un volumen de 96 mL (Figura 1 E). Los envases plásticos fueron de tipo alimenticio N °5 (polipropileno) y se taparon con una tapa que tenía una sección con tergal para la respiración y para evitar la depredación o el escape de los individuos. Dentro de cada envase, se colocó una porción de dieta natural. La dieta se cambió cada cuatro días o antes si las condiciones de consumo de las larvas así lo requerían.
El número de estadíos se registró al recolectar las cápsulas cefálicas de las mudas. El ancho de cada cápsula cefálica se midió usando la distancia entre las genas según el método Dyar (1890). También, se midió el largo del cuerpo de todos los estadíos.
Cada una de las larvas se revisó diariamente hasta alcanzar el estado de pupa. Se determinó el número de estadíos. Además, para cada estadío, se obtuvo la duración media (días), la desviación estándar (días), el ámbito (días) y el coeficiente de variación. Mientras que para las cápsulas cefálicas y el largo del cuerpo de las larvas se determinó la media (mm), la desviación estándar (mm), el ámbito (mm) y el coeficiente de variación. Un total de 30 mediciones se realizaron para cada variable biométrica definida.

Figura 1. Dieta natural usada en el laboratorio. A) secciones de hojas y tallos; B) secciones de tallos; C) secciones de tallos y raíces; D) cámaras de oviposición; E) envase para eclosión de huevos; F) cuadrícula para conteo de huevos; G) traslado de huevos a dieta para eclosión; H) envases para la crianza de L1 de S. anania.
Figure 1. Natural diet used in the laboratory. A) leaf and stem sections; B) stem sections; C) stem and root sections; D) oviposition chambers; E) containers for egg eclosion; F) egg counting grid; G) transfer of eggs to a hatching diet; H) containers for rearing L1 of S. anania.
Pupas. Se realizaron diferentes procesos de crianza con el propósito de alcanzar la totalidad de datos requeridos durante el estado de pupa. Cada una se colocó en envases plásticos redondos de 237 mL similares a los utilizados en la eclosión de huevos. Los envases plásticos fueron de tipo alimenticio N °5 (polipropileno) y se taparon con tergal para evitar la depredación.
Las pupas se revisaron diariamente y se registró la duración en días requerida para llegar hasta adulto. Se determinó la media (días), la desviación estándar (días), el ámbito (días) y el coeficiente de variación en un grupo de 30 pupas; mientras que, para las mediciones del largo del cuerpo, se determinó la media (mm), la desviación estándar (mm), el ámbito (mm) y el coeficiente de variación en un total de 30 mediciones. También, se registró la proporción de sexos de los adultos que emergieron de las 30 pupas.
Adultos. Las mediciones de los adultos se realizaron de forma independiente a 24 machos y 24 hembras. Por lo tanto, la identificación y clasificación por género, se realizó durante la etapa de pupa según los criterios descritos por Solís et al. (2019). Cada uno de los adultos se colocó en envases plásticos redondos de 237 mL. Los envases plásticos eran de tipo alimenticio N °5 (polipropileno) y se taparon con la propia tapa plástica para evitar la depredación o el escape. En el interior de los envases, se colocó algodón con miel de abeja al 10% para la alimentación de los adultos. A los adultos se les cambió la dieta cada dos días.
Los adultos se revisaron diariamente y se registró la duración en días hasta el momento de la muerte natural. Se determinó la media (días), la desviación estándar (días), el ámbito (días) y coeficiente de variación para las 24 hembras y 24 machos. Para las mediciones del largo del cuerpo y la extensión alar, se determinó la media (mm), la desviación estándar (mm), el ámbito (mm) y el coeficiente de variación para las 24 hembras y 24 machos.
Equipo de mediciones y análisis de datos. Las mediciones se realizaron con un estereomicroscopio trinocular Marca Optika Modelo SZM-LED2 con micrómetro ocular y un microscopio digital Handheld Pro, marca Celestron provisto con el programa Celestron MicroCapture Pro (California, Estados Unidos). Los datos se analizaron por medio de las variables estadísticas anotadas, usando el programa Microsoft ® Excel ® para Microsoft 365 MSO (versión 2401).
Actividad reproductiva. Para cumplir este objetivo, fue necesario contar con adultos (hembras y machos) sanos y con un día de emergidos. Por lo tanto, originalmente, se plantearon dos procedimientos para obtener las pupas: 1) recolecciones en campo y 2) crianzas en el laboratorio. En la primera, se recolectaron pupas durante recorridos semanales en el 2022. Se inspeccionaron las plantas, dando énfasis al sistema radicular y el suelo. Las plantas tenían edades entre 1 a 20 semanas después de siembra. Los materiales recolectados se colocaron en cajas plásticas cuyas tapas tenían agujeros cubiertos con tela tergal para permitir la aireación y, posteriormente, ser trasladados al laboratorio.
En el segundo procedimiento, se realizaron varios procesos de crianza durante el segundo semestre del 2022 y principio del 2023. Cada proceso inició con 200 adultos recolectados en una semana. La metodología utilizada fue la misma llevada a cabo para la determinación del ciclo de vida y descrita en los párrafos anteriores. Cada individuo fue criado desde el huevo hasta la pupa, lo que representó un proceso cuidadoso y demandante en tiempo. A partir de ese momento, se seleccionaron los adultos recién emergidos para los estudios de la cópula, oviposición y fecundidad.
Ciclo de vida y aspectos biológicos de S. anania
El estado de huevo en S. anania tuvo una duración entre 7 a 8 días. Los huevos son pequeños, ovalados y miden en promedio 0,38 mm de largo por 0,32 mm de ancho (Tabla 1). Toda la superficie del huevo presenta un aspecto reticulado, mientras que su color cambia desde el blanco perlado hasta amarillento.
Es muy notable apreciar la forma de la cápsula cefálica del L1 cuando la larva está próxima a emerger (Figura 2A). Los huevos presentaron un alto porcentaje de eclosión (93%, n = 30).
Tabla 1. Valores promedio, ámbito y coeficiente de variación para la duración desde la postura hasta la eclosión, así como el largo y ancho de los huevos de Sufetula anania (n = 30).
Table 1. Mean values, range and coefficient of variation for the duration from laying to hatching, as well as the length and width of Sufetula anania eggs (n = 30).
|
Parámetro estadístico |
|
Duración desde postura hasta eclosión (días) |
|
Largo (mm) |
|
Ancho (mm) |
|
Media ± DE* |
|
7,10 ± 0,02 |
|
0,38 ± 0,02 |
|
0,32 ± 0,02 |
|
Ãmbito |
|
7-8 |
|
0,35 - 0,43 |
|
0,29 - 0,37 |
|
CV** |
|
0,04 |
|
0,05 |
|
0,06 |
|
* Desviación estándar. ** CV = coeficiente de variación. |
||||||
La hembra no tiene un patrón definido de deposición de huevos durante la oviposición. Los huevos se encontraron ubicados de forma individual, en pares, así como en grandes masas de más de 20 unidades. Las hembras colocan los huevos en sitios de difícil acceso, por ejemplo, espacios axilares entre el tallo y las hojas o secciones vegetales con cortes mecánicos. Sin embargo, los tejidos vegetales frescos de tallos y raíces son especialmente preferidos por las hembras para la oviposición.
Originalmente, la metodología de la oviposición contemplaba el uso de materiales como tubos de PVC recubiertos con papel encerado. Sin embargo, estos materiales ni otros como papel aluminio o papel Kraft fueron atractivos para lograr la oviposición a nivel de laboratorio. Por lo tanto, se debió optar por la metodología descrita en la sección correspondiente.
Larvas
Se determinaron cinco estadíos para S. anania. El estado de larva tuvo una duración entre 15 a 39 días (Tabla 2). Las cápsulas cefálicas sirvieron como indicador del cambio entre los diferentes estadíos.
Los dos primeros estadíos registraron tamaños diminutos con una longitud promedio de 1,58 mm ± 0,14 y 2,85 mm ± 0,40 respectivamente, mientras que las longitudes promedio para los estadíos L3, L4 y L5 fueron 4,88 mm ± 1,01, 8,19 mm ± 1,73 y 13,03 mm ± 1,88 respectivamente (Tabla 2).
Tabla 2. Valores promedio, ámbito y coeficiente de variación para la longitud del cuerpo de los estadíos larvales (L1 a L5); Largo y duración de pupas a adulto de Sufetula anania (n = 30).
Table 2. Average values, range and coefficient of variation for the body length of the (L1 a L5) instars and length and duration of pupae to adult stage of Sufetula anania (n = 30).
|
Parámetro estadístico |
|
Larvas |
|
Pupas |
||||||
|
|
Longitud del cuerpo (mm) |
|
Longevidad hasta adulto (días) |
|
Largo (mm) |
|||||
|
|
|
L1 |
L2 |
L3 |
L4 |
L5 |
|
|
|
|
|
Media ± DE* |
|
1,58 ± 0,14 |
2,85 ± 0,40 |
4,88 ± 1,01 |
8,19 ± 1,73 |
13,03 ± 1,88 |
|
8,63 ± 1,3 |
|
5,78 ± 0,61 |
|
Ãmbito |
|
1,3 - 1,9 |
2,0 - 3,5 |
3,5 - 7,0 |
5,0 - 11,0 |
9,5 - 17,5 |
|
6 - 11 |
|
4,50 - 7,00 |
|
CV** |
|
0,09 |
0,14 |
0,21 |
0,21 |
0,14 |
|
0,15 |
|
0,11 |
|
* DE = Desviación estándar. ** CV = coeficiente de variación. |
||||||||||
Las larvas tienen forma cilíndrica, integumento liso y la coloración varía desde el blanco perlado (estadíos iniciales) hasta un tono amarillento (último estadío). El escudo protorácico está bien definido y su color varía desde amarillo claro hasta café claro (Figura 2 B). Todas las setas primarias son derivadas de los pináculos y todos los espiráculos están rodeados por un círculo ligeramente esclerotizado.
Las larvas se alimentaron de tejidos frescos de la planta de piña, específicamente, de secciones de tallos tiernos de la semilla vegetativa. Una observación importante durante el proceso de crianza fue el rechazo de las larvas a dietas contaminadas por hongos o levaduras. Las larvas en cualquier estadío se alimentaron de tejido vegetal fresco.
La dieta natural consistió en una fracción de tejido con una relación 50:50 entre tallo tierno y hojas tiernas (Figura 2 C). Los dos primeros estadíos se alimentaron mayoritariamente con el tejido tierno de las hojas, mientras que los estadíos L3, L4 y L5 consumieron vorazmente cualquier parte de la dieta. El hábito de consumo en el tallo inició por medio de perforaciones y continuó hasta crear túneles internos de alimentación, que al mismo tiempo le servían como lugar de refugio y protección.
Pupas
El estado de pupa tuvo una duración entre 6 a 11 días y su longitud promedio fue de 5,78 mm ± 0,61 (Tabla 2). La pupa es tipo obtecta. En este tipo de pupa, son visibles las futuras estructuras de los adultos (Figura 2 D). Otro aspecto importante es que durante el estado de pupa se pueden clasificar los géneros, particularmente, a través de la sutura genital femenina localizada en el segmento abdominal A-9 (se observa como una hendidura cefalocaudal) (Figura 3). Se determinó una mayor proporción de hembras (53%) en comparación con los machos (47%).
Durante el último estadío, las larvas reducen y cesan su alimentación como forma de preparación hacia la etapa de pupa. Las larvas L5 salen de los sitios de alimentación y conforman una envoltura con sedas y heces secas. Esta envoltura o cápsula pupal, usualmente, queda fuertemente adherida a los tejidos vegetales de alimentación. En algunos casos, las pupas quedan ubicadas en sitios de difícil localización.
Entre los cuatro estados del ciclo de vida de S. anania reproducidos en laboratorio, el estado de pupa fue el más susceptible a factores de mortalidad. Por ejemplo, condiciones de alta humedad (formación de gotas) dentro de los envases plásticos generaron una mayor mortalidad de las pupas. También, se observaron síntomas de desecación, malformaciones, presencia de ácaros depredadores, así como la germinación de hongos (no identificados).
Adultos
Bajo confinamiento, la duración promedio de vida de las hembras (7,29 días ± 2,65) fue superior a los machos (5,25 días ± 4,27). La longitud promedio del cuerpo de las hembras (5,07 mm ± 0,71) fue mayor en comparación con los machos (4,81 mm ± 0,61). De igual forma, en las hembras el promedio de la extensión alar (11,57 mm ± 1,37) fue mayor que la medida obtenida para los machos (10,49 mm ± 1,77) (Tabla 3).
El aspecto fenotípico de las hembras y los machos adultos es similar (Figura 2 E). Tanto en el cuerpo y alas, se presentan escamas de coloración grisácea y amarillentas. En ambos, las alas anteriores presentan una mancha redonda de color gris oscuro, similar a la descripción de Solís et al. (2019). Un aspecto diferenciador en los adultos es que las antenas de los machos son más gruesas en comparación con las antenas de las hembras (Figura 2 F).

Figura 2. Ciclo de vida de Sufetula anania. A) huevos; B) larva; C) dieta natural de tejido vegetal fresco; D) pupa; E) adultos durante la actividad reproductiva, en la parte superior se presenta una hembra y en la parte inferior se presenta un macho; F) macho.
Figure 2. Life cycle of Sufetula anania. A) eggs; B) larva; C) natural diet of fresh plant tissue; D) pupa; E) adults during reproductive activity, the top panel shows a female and the bottom panel shows a male; F) male.
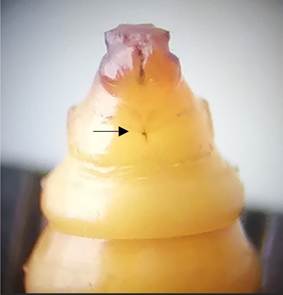
Figura 3. Sutura genital femenina en el segmento abdominal A-9.
Figure 3. Female genital suture in abdominal segment A-9.
Tabla 3. Valores promedio, ámbito y coeficiente de variación para las mediciones de longevidad, largo del cuerpo y extensión alar de las hembras y machos de Sufetula anania (n = 24).
Table 3. Mean values, range and coefficient of variation for longevity, body length and wing span measurements of females and males of Sufetula anania (n = 24).
|
Parámetro estadístico |
|
Longevidad (días) |
|
Largo del cuerpo (mm) |
|
Extensión alar (mm) |
|
|
|
|
|
|
|
|
|
|
|
Hembras |
||||
|
Media ± DE* |
|
7,29 ± 2,65 |
|
5,07 ± 0,71 |
|
11,57 ± 1,37 |
|
Ãmbito |
|
1-12 |
|
3,67 - 6,24 |
|
8,89 - 13,50 |
|
CV** |
|
0,36 |
|
0,14 |
|
0,12 |
|
|
|
Machos |
||||
|
Media ± DE* |
|
5,25 ± 4,27 |
|
4,81 ± 0,61 |
|
10,49 ± 1,77 |
|
Ãmbito |
|
1-12 |
|
3,96 - 6,23 |
|
6,74 - 13,82 |
|
CV** |
|
0,81 |
|
0,13 |
|
0,17 |
|
* Desviación estándar. ** Coeficiente de variación |
||||||
A través de las observaciones en varios procesos de crianza, se evidenciaron algunos aspectos que limitan la sobrevivencia de los adultos. Por ejemplo, algunos de los individuos no lograban salir completamente de la pupa, otros lograban salir, pero con algún tipo de malformación en su cuerpo, principalmente, en las alas. Finalmente, otro aspecto a anotar es que algunos adultos quedaban atrapados en el exceso de humedad del algodón que se usaba para la alimentación, limitándoles el vuelo y provocando una muerte prematura.
Actividad reproductiva
La recolección de pupas en campo fue descartada debido a la baja eficiencia de la labor. Por ejemplo, tres personas en labores de muestreos recolectaron menos de cinco pupas durante una jornada de trabajo. Por lo tanto, se tomó la decisión de continuar únicamente con la obtención de pupas mediante procesos de crianza, con la misma metodología que ya había sido utilizada de forma exitosa para la determinación del ciclo de vida. El cumplimiento de este objetivo presentó dos grandes dificultades: 1) las altas mortalidades de las pupas durante los ciclos de crianza impidieron alcanzar la cantidad requerida de adultos; y 2) la baja disponibilidad de insectos para iniciar los procesos de crianza debido a que las poblaciones de la plaga se redujeron en el transcurso del 2023.
Para cada nuevo proceso de crianza, fue necesario realizar la captura de al menos 200 adultos durante tres noches seguidas. Por lo tanto, todo el equipo de recolección se instaló entre 7 y 9 de la noche, momento en el cual se identificó la mayor actividad de vuelo de los insectos. Durante las jornadas, se recolectaron menos de 20 adultos; en otras ocasiones, las condiciones climáticas (lluvias y vientos) impidieron la captura y en otras no fue posible desplazarse a los sitios de recolecta debido a asignaciones laborales lejos de la región. Todos estos elementos son críticos solamente cuando hay baja incidencia de la plaga, por el contrario, cuando se dan altas incidencias no hay obstáculos para capturar rápidamente los insectos requeridos.
En el segundo semestre del 2022, se instalaron tres procesos de crianza a pesar de las bajas poblaciones del insecto. En el 2023, la presencia en campo prácticamente desapareció. De los últimos tres procesos de crianza, solamente emergieron 2 o 3 adultos sanos. La mayoría de las pupas nunca cambiaron a adulto.
Discusión
Los estudios de carácter biológico deben basarse en el conocimiento de sus características, ya que representan una herramienta clave para el manejo de toda plaga. Su importancia radica en la caracterización del crecimiento y desarrollo de los individuos de una población, que conduce a un proceso de toma de decisiones dentro del manejo agroecológico de una plaga (Umaña y Carballo 1995, Soto-Manitiu et al. 1997, Arias Reverón 1988, Castillo et al 2014). En este estudio, se determinaron los principales aspectos biológicos de la plaga S. anania: ciclo de vida, parámetros biométricos y una metodología de crianza en laboratorio compuesta por secciones de tallos de semilla vegetativa de piña.
La disponibilidad de trabajos de investigación referentes al género Sufetula spp. es escasa y antigua, lo que limita la comparación entre las especies (Hayden 2013, Genty y Mariau 1975). Se determinó que S. anania pasa por cuatro estados de desarrollo: huevo, larvas, pupa y adulto. Genty y Mariau (1975) determinaron la duración del ciclo de vida de S. diminutalis entre 28 y 31 días (no se reportó temperatura ni humedad relativa), lo cual es menor a los datos generados para S. anania en esta investigación: 29 a 70 días (temperatura promedio 25,1 °C, humedad relativa 83%). Se presentó una similitud en la edad de los huevos, para S. diminutalis entre 8 a 10 días, en comparación con los 7 a 8 días para S. anania. Ambas especies también coinciden en sus cinco estadíos, sin embargo, varían en la duración: S. diminutalis (entre 13 y 14 días) y S. anania (entre 15 y 39 días). La duración del estado de pupa fue similar: S. diminutalis (9 días) y S. anania (11 días). En investigaciones más recientes (Cruz y Obando 2021) determinaron el ciclo de vida para S. anania con un promedio de 57 días y cuatro estadíos que sumaron 23 días, datos que fueron similares a la presente investigación, en donde se determinó el ciclo de vida con un promedio de 40 días, de los cuales 24 fueron para las larvas. Sin embargo, en esta investigación, se determinaron cinco estadíos larvales.
Metodología de crianza, dieta natural y comportamiento de S. anania
Actualmente, hay escasos reportes disponibles que incluyan una metodología de crianza para S. anania. Sin embargo, Genty y Mariau (1975) y Genty et al. (1976) desarrollaron algunos trabajos similares para la plaga S. diminutalis. En la metodología, utilizaron raíces jóvenes de palma aceitera dentro de un tubo de vidrio enterrado en la arena para que el proceso de crianza tuviera lugar en completa oscuridad.
En este estudio, la metodología de crianza de S. anania para determinar el ciclo de vida se realizó de forma exitosa siguiendo el fotoperiodo natural de Costa Rica, por lo tanto, no se considera como un requisito obligatorio para la crianza utilizar una condición de completa oscuridad. Sin embargo, bajo condiciones naturales, es muy posible que el desarrollo de las larvas ocurre en completa oscuridad. El resto de la metodología de crianza para S. diminutalis la realizaron con raíces de palma aceitera, en contraste, para S. anania, una vez cortadas las raíces de la planta de piña, estas se descomponen rápidamente, lo que impide que sea un material adecuado para la crianza.
Las hembras tienen la habilidad de colocar los huevos en grupos de diferentes cantidades, así como en sitios de difícil acceso (Figura 3 A y B). Se observó la oviposición en diversos órganos de las plantas de piña (tales como raíces, tallos, parte aérea y en la base de las hojas), lo cual demuestra la adaptación que ha tenido la especie a este cultivo (Solís et al. 2019). El alto porcentaje de eclosión de los huevos (93%) le confiere una ventaja en su proceso reproductivo.
El estado larval es el más dañino durante el ciclo de vida de S. anania, donde se observó la preferencia hacia los tejidos vegetales tiernos y libres de contaminación (Figura 1 C). Por lo tanto, sería poco usual encontrar la plaga reproduciéndose sobre tejidos en algunas etapas finales del ciclo de cultivo como la derriba de la plantación o el barbecho. Caso contrario se presenta en otra plaga importante en el cultivo de piña, Stomoxys calcitrans L. (Diptera; Muscidae), la cual se reproduce en los residuos y rastrojos de piña (Blanco-Metzler y Arguedas Marín 2015). Los primeros daños de esta plaga se reportaron en raíces tiernas de la planta de piña (Figura 3 D), sin embargo, la plaga puede completar su ciclo de vida en otros órganos de la planta, como los tallos y hojas (SFE 2018).
Cuando se estudia una plaga emergente, es necesario conducir estudios detallados que permitan el descubrimiento de algunos aspectos biológicos como el ciclo de vida y su comportamiento alimenticio (Chacón Castro et al. 2009).
S. anania es una especie de tamaño diminuto, lo que confiere una mayor complejidad para encontrarla e identificarla en el campo. Los hallazgos de esta investigación permitieron: describir una metodología de crianza que puede ser usada como base para pruebas de eficacia biológica y caracterizar el ciclo de vida completo, además, conocer que la plaga tiene un comportamiento esquivo en donde los insecticidas de contacto quizás no sean la mejor opción de manejo.
Se sugiere que los nuevos proyectos de investigación incluyan la determinación del comportamiento reproductivo, la identificación de los hospederos alternos, así como la identificación de los enemigos naturales.
Conclusión
Esta investigación determinó que la plaga S. anania tiene un ciclo de vida compuesto de 4 estados de desarrollo (huevo, larva, pupa y adulto) con una duración entre 29 a 70 días. El patrón de oviposición es variable, desde un huevo por postura, en pares y hasta en masas de 20 huevos. El estado larval es el más dañino y el estado de pupa el que presentó la mayor mortalidad durante la cría en el laboratorio. Se desarrolló una metodología de crianza en laboratorio compuesta por secciones de tallos de semilla vegetativa de piña. La dieta natural desinfectada y los factores ambientales fueron elementos fundamentales en el desarrollo de la metodología de cría en el laboratorio. Durante su alimentación, las larvas generan túneles dentro de los tejidos vegetales que les sirven como sitios de refugio y protección. Para un monitoreo de la plaga en el campo, los primeros daños de S. anania se presentan en raíces tiernas de la planta de piña ubicada en la periferia de la plantación.
Literatura citada
Arias Reverón, JM. 1988. Aspectos de la biología y la ecología de las poblaciones de la escama coma Lepidosaphes beckii (Newmann) y la escama fina L. gloveri (Packard) (Homoptera: Diaspididae), plagas de los cultivos de cítricos en Costa Rica. Tesis M.Sc. San José, Costa Rica, Universidad de Costa Rica. 122 p.
Bartholomew, DP; Paull, RE; Rohrbach, KG. 2003. The pineapple: botany, production and uses. Londres, Reino Unido, CABI Publishing. 301 p.
Blanco-Metzler, H; Arguedas-Marín, A. 2015. Efecto del color de trampa y tipo de adherente en la captura de Stomoxys calcitrans (L.) (Diptera: Muscidae) en el cultivo de piña (Ananas comosus) (L.) Merr. Entomología Mexicana 2:312-318.
Blanco-Metzler, H; Watt, A; Cosens, D. 1993. Ciclo de vida y comportamiento de oviposición de Ecdytolopha torticornis (Lep: Tortricidae) barrenador de la nuez de la macadamia. Manejo Integrado de Plagas 29:36-39.
Bonneau, X; Husni, M; Beaudoin-Oliver, L; Susilo, J. 2007. Controlling Sufetula spp.: a coconut insect pest on peat soils. Experimental Agriculture 43:289-299.
Bonneau, X; Husni, M; Philippe, R; Somchit, N; Jourdan, C; Lubis, N. 2004. Discovery of a factor limiting yields in a coconut plantation on Peat: the insect pest Sufetula spp. Experimental Agriculture 40:53-64.
CANAPEP (Cámara de Exportadores y Productores de Piña). 2024. Estadísticas de la Cámara de Exportadores y Productores de Piña. Costa Rica. s. p.
Castillo, A; Johnson, MT; Badenes-Pérez, FR. 2014. Biology, behavior, and larval morphology of Salbia lotanalis (Lepidoptera: Crambidae), a potential biological control agent of Miconia calvescens (Myrtales: Melastomataceae) from Costa Rica. Annals of the Entomological Society of America 107(6):1094-1101.
Castro, Z. 2019. El sistema agroindustrial de la piña en Costa Rica. IX International Pineapple Symposium. ISHS Acta Horticulturae 1239. La Habana, Cuba. 8 p.
Chacón Castro, Y; Garita Rojas, C; Vaglio Cedeño, C; Villalba Velászquez, V. 2009. Desarrollo de una metodología de crianza en laboratorio del gusano cogollero del maíz Spodoptera frugiperda (Smith) (Lepidoptera: Noctuidae) como posible hospedante de insectos biocontroladores de interés agrícola. Tecnología en Marcha 22(4):28-37.
Cruz, AE; Obando, JD. 2021. Alternativas de control, identificación de signos y síntomas comportamiento biológico y consumo de raíz de piña (Ananas comosus var. comosus) híbrido MD-2 del barrenador de raíz Sufetula anania (LEP:Crambidae) en Costa Rica. Revista Científica LIFE-RID 2021:51-58.
Dyar, HG. 1890. The number of molts of lepidopterous larvae. Psyche 4:420-422.
Genty, P; Desmier, R; Mariau, D. 1976. Infestation des racines aériennes du palmier à huile par des chenilles genre Sufetula Walker (Lépidoptère: Pyralidae). Oléagineux 31(8-9):365-370.
Genty, P; Mariau, D. 1975. Morphologie et biologie du Pyralidae des racines de l'Elaeis, Sufetula diminutalis. Oléagineux 30(4):147-152.
Hayden, JE. 2013. Sufetula Walker in Florida (Lepidoptera: Crambidae). In Insecta Mundi 801. Consultado 18 set. 2022. Disponible en http://digitalcommons.unl.edu/insectamundi/801
Hilje, L; Saunders, JL. 2008. Manejo integrado de plagas en Mesoamérica: aportes conceptuales. Cartago, Costa Rica. Editorial Tecnológica de Costa Rica. 714 p.
Nielsen, V. 1998. Procedimientos biológicos para reducir el uso de plaguicidas y mejorar la agricultura tropical. Boltec 28(1):69-77.
Nuss, M; Landry, B; Mally, R; Vegliante, F; Trȁnker, A; Bauer, F; Hayden, J; Segerer, A; Schouten, R; Li, H; Trofimova, T; Solis, MA; De Prins; Speidel, W. 2022. Global information system on Pyraloidea. Consultado 18 set. 2022. Disponible en http://globiz.pyraloidea.org/Pages/Reports/TaxonReport.aspx
SFE (Servicio Fitosanitario del Estado, Costa Rica). 2018. €œCabeza roja €. Unidad Operativa Regional Huetar Norte. San Carlos, Costa Rica. 19 p.
Solís, MA; Hayden, JE; Sanabria, F; González, F; Sanabria, C; Gulbronson, CJ. 2019. A new species of Sufetula Walker (Lepidoptera: Crambidae) feeding on the roots of pineapple, Ananas comosus (L.) (Bromeliaceae), from Costa Rica. Proceedings of the Entomological Society of Washington 121(3):497-510.
Soto-Manitiu, J; Chaverri, LG; Jirón, LF. 1997. Notas sobre la biología y la ecología de Anastrepha obliqua (Diptera: Tephritidae), plaga de plantas anacardiáceas en América Tropical, I. Formas Inmaduras. Agronomía Mesoamericana 8(2):116-120.
Umaña, E; Carballo, M. 1995. Biología de Antiteuchus tripterus L. (Hemiptera: Pentatomidae) y su parasitoide Trissolcus radix Johnson (Hymenoptera: Scelionidae) en macadamia. Manejo Integrado de Plagas 38:16-19.
Vandermeer, JH; Goldberg, DE. 2013. Population ecology: first principles. Second edition. Oxford, England. Princeton University Press. 304 p.
