Subpoblaciones morfométricas de espermatozoides epididimarios del venado de cola blanca (Odocoileus virginianus peruvianus)
DOI:
https://doi.org/10.15517/am.v33i2.46938Palabras clave:
semen de venado, CASA morph, reproducción aniaml, recursos genéticos silvestres de animalesResumen
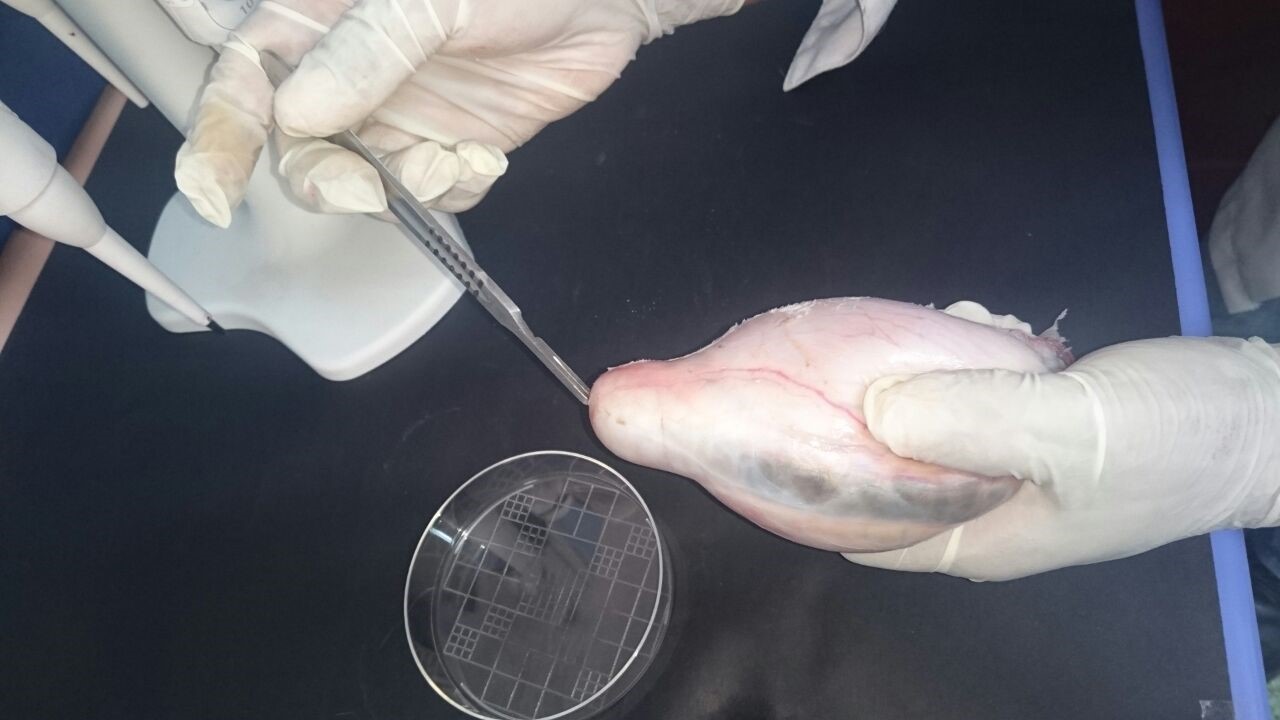
Introducción. El estudio de la morfometría espermática del venado cola blanca (Odocoileus virginianus peruvianus) permite caracterizar las células espermáticas de esta especie con propósitos de conservación. Objetivo. Determinar las subpoblaciones espermáticas según la morfometría de los espermatozoides epididimarios del venado de cola blanca, con un sistema CASA-Morph. Materiales y métodos. El estudio se desarrolló en el segundo semestre 2016, en la Universidad Nacional de San Antonio Abad del Cusco, Perú. En muestras de semen obtenidas del extremo caudal del epidídimo de dos venados (dos y cuatro dientes), se determinó con base en el sistema CASA-Morph, Integrated Semen Analysis System (ISAS®v1): la longitud, anchura, área, perímetro, elipticidad, elongación, regularidad y rugosidad de la cabeza del espermatozoide, también, la anchura, área, distancia y ángulo de inserción de la pieza intermedia. Se realizó un análisis de componentes principales (PCA) y se aplicó el modelo no jerárquico k-medias para determinar el número óptimo de clústeres. Resultados. Las variables morfométricas se distribuyeron en cinco PCA: elipticidad, tamaño, circularidad, ángulo de inserción de la pieza intermedia y anchura de la pieza intermedia, que explicaron un 81,24 % de la varianza total. El análisis de clústeres determinó cuatro subpoblaciones (SP), la SP1 agrupó células grandes, alargadas con alta elongación y elipticidad (21,76 %), la SP2 compuesta por espermatozoides de tamaño pequeño y delgados tanto en la cabeza como en la pieza intermedia (37,7 %), la SP3 se relacionó con la presencia de células alargadas con valores altos de anchura de la pieza intermedia, elipticidad y elongación (17,7 %), y la SP4 agrupó espermatozoides de tamaño intermedio de la cabeza y de la pieza intermedia (22,84 %). Conclusiones. La determinación de cuatro subpoblaciones espermáticas en el semen de venado cola blanca puede ser la base de programas de reproducción asistida de esta especie.
Descargas
Citas
Ake-Lopez, J., Cavazos-Arizpe, E., Magana-Monforte, J. G., Centurion-Castro, F., & Silva-Mena, C. (2010). Effect of age and postmortem time on some White-Tailed deer (Odocoileus virginianus texanus) epididymal sperm characteristics and response of cryopreservation. American Journal of Animal and Veterinary Sciences, 5(3), 183–186. https://doi.org/10.3844/ajavsp.2010.183.186https://doi.org/10.3844/ajavsp.2010.183.186
Barquero, V., Roldan, E. R. S., Soler, C., Yániz, J. L., Camacho, M., & Valverde, A. (2021). Predictive Capacity of Boar Sperm Morphometry and Morphometric Sub-Populations on Reproductive Success after Artificial Insemination. Animals, 11(4), Article 920. https://doi.org/10.3390/ani11040920
Barquero, V., Víquez, L., Calderón-Calderón, J. C., & Valverde, A. (2021). Optimal frame rate to evaluate boar sperm kinematic with a CASA-Mot system. Agronomía Mesoamericana, 32(1), 1–18. https://doi.org/10.15517/am.v32i1.41928
Belleannée, C., Thimon, V., & Sullivan, R. (2012). Region-specific gene expression in the epididymis. Cell and Tissue Research, 349, 717–731. https://doi.org/10.1007/s00441-012-1381-0
Beracochea, F., Gil, J., Sestelo, A., Garde, J. J., Santiago-Moreno, J., Fumagalli, F., & Ungerfeld, R. (2014). Sperm characterization and identification of sperm sub-populations in ejaculates from pampas deer (Ozotoceros bezoarticus). Animal Reproduction Science, 149(3–4), 224–230. https://doi.org/10.1016/j.anireprosci.2014.07.013
Cooper, T. G., & Yeung, C. -H. (2006). Sperm maturaiton in the human epididymis. In C. J. De Jonge & C. Barratt (Eds.), The sperm cell production, maturation, fertilization, regeneration (pp. 72–107). Cambridge University Press. https://doi.org/10.1017/CBO9780511545115.005
Cornwall, G. A. (2009). New insights into epididymal biology and function. Human Reproduction Update, 15(2), 213–227. https://doi.org/10.1093/humupd/dmn055
Cucho, H., Gallegos, M., Ccoiso, R., Meza, A., Ampuero, E., Ordóñez, C., & Valverde, A. (2021). Morphometry and subpopulation of llama (Lama glama) sperm using the ISAS® CASA-Morph system. Revista de Investigaciones Veterinarias Del Peru, 32(1), Article e19506. https://doi.org/10.15381/RIVEP.V32I1.19506
Cucho, H., López, Y., Caldeira, C., Valverde, A., Ordóñez, C., & Soler, C. (2019). Comparison of three different staining methods for the morphometric characterization of Alpaca (Vicugna pacos) sperm , using ISAS ® CASA-Morph system. Nova Biologica Reperta, 6(3), 284–291. https://doi.org/10.29252/nbr.6.3.284
Curry, M. R. (2000). Cryopreservation of semen from domestic livestock. Reviews of Reproduction, 5(1), 46–52. https://doi.org/10.1530/ror.0.0050046
Downing-Meisner, A., Klaus, A. V., & O’Leary, M. A. (2005). Sperm head morphology in 36 species of artiodactylans, perissodactylans, and cetaceans (Mammalia). Journal of Morphology, 263(2), 179–202. https://doi.org/10.1002/jmor.10297
Esteso, M. C., Fernández-Santos, M. R., Soler, A. J., Montoro, V., Martínez-Pastor, F., & Garde, J. J. (2009). Identification of sperm-head morphometric subpopulations in iberian red deer epididymal sperm samples. Reproduction in Domestic Animals, 44(2), 206–211. https://doi.org/10.1111/j.1439-0531.2007.01029.x
Esteso, M. C., Rodríguez, E., Toledano-Díaz, A., Castaño, C., Pradiee, J., López-Sebastián, A., & Santiago-Moreno, J. (2015). Descriptive analysis of sperm head morphometry in Iberian ibex (Capra pyrenaica): Optimum sampling procedure and staining methods using Sperm-Class Analyzer®. Animal Reproduction Science, 155(1), 42–49. https://doi.org/10.1016/j.anireprosci.2015.01.014
Esteso, M. C., Soler, A. J., Fernández-Santos, M. R., Quintero-Moreno, A. A., & Garde, J. J. (2006). Functional significance of the sperm head morphometric size and shape for determining freezability in Iberian red deer (Cervus elaphus hispanicus) epididymal sperm samples. Journal of Andrology, 27(5), 662–670. https://doi.org/10.2164/jandrol.106.000489
Esteso, M. C., Toledano-Díaz, A., Castaño, C., Pradiee, J., Lopez-Sebastián, A., & Santiago-Moreno, J. (2018). Effect of two cooling protocols on the post-thaw characteristics of Iberian ibex sperms. Cryobiology, 80(1), 12–17. https://doi.org/10.1016/j.cryobiol.2018.01.003
Gaddum, P. (1968). Sperm maturation in the male reproductive tract: Development of motility. The Anatomical Record, 161(4), 471–482. https://doi.org/10.1002/ar.1091610409
Gage, M. (1998). Mammalian sperm morphometry. Proceedings of the Royal Society B: Biological Sciences, 265(1391), 97–103. https://doi.org/10.1098/rspb.1998.0269
Ministerio de Desarrollo Agrario y Riego del Perú. (2014). Decreto Supremo que aprueba la actualización de la lista de clasificación y categorización de las especies amenazadas de fauna silvestre legalmente protegidas (Nº 004-2014-MINAGRI). Organización de las Naciones Unidas para la Alimentación y la Agricultura. http://extwprlegs1.fao.org/docs/pdf/per132692.pdf
Hernández-Corredor, L., Silva-Torres, A., Celis-Alba, D., Landaeta-Hernández, A., & Rubio-Parada, J. (2018). Evaluación de la motilidad y morfometría en espermatozoides descongelados de venado cola blanca (Odocoileus virginianus). ResearchGate. https://n9.cl/w5eb8
Hidalgo, M., Rodríguez, I., Dorado, J., & Soler, C. (2008). Morphometric classification of Spanish thoroughbred stallion sperm heads. Animal Reproduction Science, 103(3–4), 374–378. https://doi.org/10.1016/j.anireprosci.2007.06.001
Kaiser, H. F. (1958). The varimax criterion for analytic rotation in factor analysis. Psychometrika, 23(3), 187–200. https://doi.org/10.1007/BF02289233
Kaufman, L., & Rousseeuw, P. J. (2005). Finding groups in data : an introduction to cluster analysis. John Wiley Sons, Inc., Publications. https://doi.org/10.1002/9780470316801
Kirschner, S. M., & Rodenkirch, R. (2017). Assessment of butorphanol-azaperone-medetomidine combination as anesthesia for semen collection and evaluation of semen quality in white-tailed deer (Odocoileus virginianus). Animal Reproduction Science, 184(1), 196–203. https://doi.org/10.1016/j.anireprosci.2017.07.016
Maroto-Morales, A., García-Álvarez, O., Ramón, M., Martínez-Pastor, F., Fernández-Santos, M. R., Soler, A., & Garde, J. J. (2016). Current status and potential of morphometric sperm analysis. Asian Journal of Andrology, 18(6), 863–870. https://doi.org/10.4103/1008-682X.187581
Martí, J. I., Aparicio, I. M., Leal, C. L. V., & García-Herreros, M. (2012). Seasonal dynamics of sperm morphometric subpopulations and its association with sperm quality parameters in ram ejaculates. Theriogenology, 78(3), 528–541. https://doi.org/10.1016/j.theriogenology.2012.02.035
Martinez-Pastor, F., Diaz-Corujo, A. R., Anel, E., Herraez, P., Anel, L., & de Paz, P. (2005). Post mortem time and season alter subpopulation characteristics of Iberian red deer epididymal sperm. Theriogenology, 64(4), 958–974. https://doi.org/10.1016/j.theriogenology.2005.01.003
Martinez-Pastor, F., Garcia-Macias, V., Alvarez, M., Chamorro, C., Herraez, P., de Paz, P., & Anel, L. (2006). Comparison of two methods for obtaining spermatozoa from the cauda epididymis of Iberian red deer. Theriogenology, 65(3), 471–485. https://doi.org/10.1016/j.theriogenology.2005.05.045
Martinez-Pastor, F., Garcia-Macias, V., Alvarez, M., Herraez, P., Anel, L., & de Paz, P. (2005). Sperm Subpopulations in Iberian Red Deer Epididymal Sperm and Their Changes Through the Cryopreservation Process. Biology of Reproduction, 72(2), 316–327. https://doi.org/10.1095/biolreprod.104.032730
Murtagh, F., & Legendre, P. (2014). Ward’s Hierarchical Agglomerative Clustering Method: Which Algorithms Implement Ward’s Criterion? Journal of Classification, 31(3), 274–295. https://doi.org/10.1007/s00357-014-9161-z
Orgebin-Crist, M. C. (1967). Sperm maturation in rabbit epididymis. Nature, 216(5117), 816–818. https://doi.org/10.1038/216816a0
Pacheco, V., Cadenillas, R., Salas, E., Tello, C., & Zeballos, H. (2009). Diversidad y endemismo de los mamíferos del Perú. Revista Peruana de Biología, 16(1), 5–32. https://doi.org/10.15381/rpb.v16i1.111
Peña, F., Saravia, F., García-Herreros, M., Núñez-Martínez, I., Tapia, J., Johannisson, A., Wallgren, M., & Rodríguez-Martínez, H. (2005). Identification of sperm morphometric subpopulations in two different portions of the boar ejaculate and its relation to postthaw quality. Journal of Andrology, 26(6), 716–723. https://doi.org/10.2164/jandrol.05030
Peña Hernández, A. E. (2014). Evaluación objetiva de la motilidad de los espermatozoides epididimarios de ciervo ibérico. Relaciones con la congelabilidad y la calidad del semen [Tesis de Doctorado, Universidad de Castilla-La Mancha]. Repositorio institucional del Consejo Superior de Investigaciones Científicas. https://digital.csic.es/handle/10261/147311
Ramírez Lozano, R. G. (2012). Alimentación Del Venado Cola Blanca: Biología y Ecología Nutricional. Palibrio.
Ramón, M., Martínez-Pastor, F., García-Álvarez, O., Maroto-Morales, A., Soler, A. J., Jiménez-Rabadán, P., Fernández-Santos, M. R., Bernabéu, R., & Garde, J. J. (2012). Taking advantage of the use of supervised learning methods for characterization of sperm population structure related with freezability in the Iberian red deer. Theriogenology, 77(8), 1661–1672. https://doi.org/10.1016/j.theriogenology.2011.12.011
Ramón, M., Soler, A. J., Ortiz, J. A., García-Alvarez, O., Maroto-Morales, A., Roldan, E. R. S., & Garde, J. J. (2013). Sperm population structure and male fertility: An intraspecific study of sperm design and velocity in Red Deer. Biology of Reproduction, 89(5), 1-7. https://doi.org/10.1095/biolreprod.113.112110
Robaire, B., Hinton, B., & Orgebin-Crist, M. (2015). Knobil and Neill’s Physiology of Reproduction. In T. M. Plant & A. J. Zeleznik (Eds.), Physiology of reproduction (4th Ed., pp. 691–771). Elsevier Academic Press. https://doi.org/https://doi.org/10.1016/B978-0-12-397175-3.15001-X.
Soler, C., Alambiaga, A., Martí, M. A., García-Molina, A., Valverde, A., Contell, J., & Campos, M. (2017). Dog sperm head morphometry: its diversity and evolution. Asian Journal of Andrology, 19(2), 149–153. https://doi.org/10.4103/1008-682X.189207
Soler, C., Contell, J., Bori, L., Sancho, M., García-Molina, A., Valverde, A., & Segarvall, J. (2017). Sperm kinematic, head morphometric and kinetic-morphometric subpopulations in the blue fox (Alopex lagopus). Asian Journal of Andrology, 19(2), 154–159. https://doi.org/10.4103/1008-682X.188445
Soler, C., Cooper, T., Valverde, A., & Yániz, J. (2016). Afterword to Sperm morphometrics today and tomorrow special issue in Asian Journal of Andrology. Asian Journal of Andrology, 18(6), 895–897. https://doi.org/10.4103/1008-682X.188451
Soler, C., Gadea, B., Soler, A., Fernández-Santos, M., Esteso, M., Núñez, J., Moreira, P., Núñez, M., Gutiérrez, R., Sancho, M., & Garde, J. (2005). Comparison of three different staining methods for the assessment of epididymal red deer sperm morphometry by computerized analysis with ISAS®. Theriogenology, 64(5), 1236–1243. https://doi.org/10.1016/j.theriogenology.2005.02.018
Souza, T. (2009). Avaliação andrológica e criopreservação de sêmen de pumas (Puma concolor Linnaeus, 1771) adultos. [Magister Dissertation, Universidad Federal de Viçosa] Repositório do Universidad Federal de Viçosa. https://www.locus.ufv.br/bitstream/123456789/4980/1/texto%20completo.pdf
Spencer, N. H. (2013). Essentials of multivariate data analysis. Chapman and Hall/CRC Press. https://doi.org/10.1201/b16344
Thurston, L., Watson, P., Mileham, A., & Holt, W. (2001). Morphologically distinct sperm subpopulations defined by Fourier shape descriptors in fresh ejaculates correlate with variation in boar semen quality following cryopreservation. Journal of Andrology, 22(3), 382–394. http://www.ncbi.nlm.nih.gov/pubmed/11330638
Tuset, V. M., Dietrich, G. J., Wojtczak, M., Słowińska, M., de Monserrat, J., & Ciereszko, A. (2008). Comparison of three staining techniques for the morphometric study of rainbow trout (Oncorhynchus mykiss) spermatozoa. Theriogenology, 69(8), 1033–1038. https://doi.org/10.1016/j.theriogenology.2008.01.012
Valverde, A., Arenán, H., Sancho, M., Contell, J., Yániz, J., Fernández, A., & Soler, C. (2016). Morphometry and subpopulation structure of Holstein bull spermatozoa: variations in ejaculates and cryopreservation straws. Asian Journal of Andrology, 18(6), 851–857. https://doi.org/10.4103/1008-682X.187579
Valverde, A., Barquero, V., & Soler, C. (2020). The application of computer-assisted semen analysis (CASA) technology to optimise semen evaluation. A review. Journal of Animal and Feed Sciences, 29(3), 189–198. https://doi.org/10.22358/jafs/127691/2020
Valverde, A., Castro-Morales, O., Madrigal-Valverde, M., Camacho, M., Barquero, V., Soler, C., & Roldan, E. R. S. (2021). Sperm kinematic subpopulations of the American crocodile (Crocodylus acutus). PLOS ONE, 16(3), Article e0248270. https://doi.org/10.1371/journal.pone.0248270
Valverde, A., Castro-Morales, O., Madrigal-Valverde, M., & Soler, C. (2019). Sperm kinematics and morphometric subpopulations analysis with CASA systems: A review. Revista de Biología Tropical, 67(6), 1473–1487. https://doi.org/10.15517/rbt.v67i6.35151
Valverde, A., Madrigal-Valverde, M., Camacho-Calvo, M., Zambrana-Jiménez, A., & López, L. (2018). Efecto de la composición racial sobre la calidad espermática de verracos. Agronomía Mesoamericana, 29(3), 485–506. https://doi.org/10.15517/ma.v29i3.32445
Valverde, A., Madrigal-Valverde, M., Castro-Morales, O., Gadea-Rivas, A., Johnston, S., & Soler, C. (2019). Kinematic and head morphometric characterisation of spermatozoa from the Brown Caiman (Caiman crocodilus fuscus). Animal Reproduction Science, 207(1), 9–20. https://doi.org/10.1016/J.ANIREPROSCI.2019.06.011
Víquez, L., Barquero, V., Soler, C., Roldan, E. R. S., & Valverde, A. (2020). Kinematic Sub-Populations in Bull Spermatozoa: A Comparison of Classical and Bayesian Approaches. Biology, 9(6), 138–154. https://doi.org/10.3390/biology9060138
Yániz, J. L., Palacín, I., Vicente-Fiel, S., Sánchez-Nadal, J. A., & Santolaria, P. (2015). Sperm population structure in high and low field fertility rams. Animal Reproduction Science, 156, 128–134. https://doi.org/10.1016/j.anireprosci.2015.03.012
Yániz, J. L., Soler, C., & Santolaria, P. (2015). Computer assisted sperm morphometry in mammals: A review. Animal Reproduction Science, 156, 1–12. https://doi.org/10.1016/J.ANIREPROSCI.2015.03.002
Yániz, J. L., Vicente-Fiel, S., Soler, C., Recreo, P., Carretero, T., Bono, A., Berné, J. M., & Santolaria, P. (2016). Comparison of different statistical approaches to evaluate morphometric sperm subpopulations in men. Asian Journal of Andrology, 18(6), 819–823. https://doi.org/10.4103/1008-682X.186872
Archivos adicionales
Publicado
Cómo citar
Número
Sección
Licencia
1. Política propuesta para revistas de acceso abierto
Los autores/as que publiquen en esta revista aceptan las siguientes condiciones:
- Los autores/as conservan los derechos morales de autor y ceden a la revista el derecho de la primera publicación, con el trabajo registrado con la licencia de atribución, no comercial y sin obra derivada de Creative Commons, que permite a terceros utilizar lo publicado siempre que mencionen la autoría del trabajo y a la primera publicación en esta revista, no se puede hacer uso de la obra con propósitos comerciales y no se puede utilizar las publicaciones para remezclar, transformar o crear otra obra.
- Los autores/as pueden realizar otros acuerdos contractuales independientes y adicionales para la distribución no exclusiva de la versión del artículo publicado en esta revista (p. ej., incluirlo en un repositorio institucional o publicarlo en un libro) siempre que indiquen claramente que el trabajo se publicó por primera vez en esta revista.
- Se permite y recomienda a los autores/as a publicar su trabajo en Internet (por ejemplo en páginas institucionales o personales) antes y durante el proceso de revisión y publicación, ya que puede conducir a intercambios productivos y a una mayor y más rápida difusión del trabajo publicado (vea The Effect of Open Access).